L-Arginin ist eine der metabolisch vielseitigsten Aminosäuren. Neben seiner Rolle bei der Synthese von Stickstoffmonoxid dient L-Arginin als Vorstufe für die Synthese von Polyaminen, Prolin, Glutamat, Kreatin, Agmatin und Harnstoff. Verschiedene Studien an Menschen und Tieren haben gezeigt, dass die Einnahme von exogenem L-Arginin mehrere vorteilhafte pharmakologische Wirkungen hat, wenn es in Dosen eingenommen wird, die über der normalen Nahrungsaufnahme liegen.
Diese Wirkungen umfassen:
L-Arginin ist eine natürlich vorkommende basische Aminosäure. Ihr Vorkommen in Säugetierproteinen wurde 1895 von Hedin entdeckt.
Abb. 1. Überblick über den Argininstoffwechsel bei Säugetieren. Nur Enzyme, die Arginin, Ornithin oder Citrullin direkt verwenden oder herstellen, werden identifiziert, und nicht alle Reaktanten und Produkte sind gezeigt. Die Inhibition spezifischer Enzyme ist durch gestrichelte Linien und der Strich innerhalb eines Kreises angegeben. Aminosäurereste innerhalb von Proteinen werden durch Klammern identifiziert.
Abkürzungsschlüssel: ADC, Arginindecarboxylase; AGAT, Arginin: Glycinamidinotransferase; ARG, Arginase; ASL, Argininosuccinatlyase; ASS, Argininosuccinat-Synthetase; DDAH, Dimethylarginin-Dimethylaminohydrolase; Me2, Dimethyl; OAT, Ornithin-Aminotransferase; ODC, Ornithindecarboxylase; OTC, Ornithin-Transcarbamylase; P5C, 1-D1-Pyrrolin-5-carboxylat; PRMT, Protein-Arginin-Methyltransferase
Es ist erwähnenswert, dass die in Abb. 1 beschriebenen Prozesse nicht alle innerhalb jeder Zelle auftreten; stattdessen werden sie differentiell in Abhängigkeit von Zelltyp, Alter und Entwicklungsstadium, Ernährung und Gesundheitszustand oder Krankheit exprimiert. In der Tat ist Abb. 1 insofern etwas irreführend, als sie den Metabolismus von Arginin auf der Ebene des ganzen Körpers zusammenfasst; es repräsentiert nicht den Arginin-Metabolismus in irgendeinem bestimmten Zelltyp, noch zeigt es an, welche Enzyme unter verschiedenen Bedingungen exprimiert werden, welche Enzyme reguliert sind, das Vorhandensein von verschiedenen inter- und intrazellulären Transportsystemen oder wie Substrate in die verschiedenen Wege unterteilt sind.
L-Arginin und der Magen-Darm-Trakt
Es wurde wiederholt gezeigt, dass NO-Donoren die Magenschleimhaut vor Schäden schützen, die durch verschiedene Mittel hervorgerufen werden. Darüber hinaus haben Berichte aus verschiedenen Laboratorien die Bedeutung von endogenem NO beim Schutz der Magenschleimhaut gezeigt.
Zwei Studien aus Piques Labor haben gezeigt, dass NO eine vasodilatatorische Rolle in der Mikrozirkulation des Magens während der Säuresekretion spielt. Andere Studien haben die Rolle von NO als endogener Modulator der Leukozytenadhäsion anerkannt. Calatayud et al. haben gezeigt, dass transdermales Nitroglycerin gegen Indomethacin-induzierte Magengeschwüre geschützt ist, durch Aufrechterhaltung des mukosalen Blutflusses und Reduktion von Leukozyten-Endothelzell-Rolling und Adhärenz. Darüber hinaus hat Wallace festgestellt, dass die Verringerung der Magendurchblutung der wichtigste prädisponierende Faktor bei der Induktion von nicht-steroidalen entzündungshemmenden Arzneimitteln (NSAID) Gastropathie ist. Anders als die Rolle von NO bei der Aufrechterhaltung des Blutflusses kann NO durch die Förderung der Prostaglandinsynthese vor NSAID-Schäden schützen. Eine gegenseitige Wechselwirkung wurde zwischen NOS- und Cyclooxygenase (COX) -Enzymen beobachtet. Es wurde gezeigt, dass NO-Donoren die COX-Aktivität verstärken, wohingegen NOS-Inhibitoren die Prostaglandin E2 (PGE2) -Produktion blockieren.
In einer Studie aus unserem Labor demonstrierten wir die Rolle von NO beim Schutz gegen Indomethacin-induzierte Magengeschwüre. Intraperitoneale (i.p.) Injektion von L-Arginin (300 mg/kg) 30 Minuten vor i.p. Die Injektion von 30 mg/kg Indomethacin an Ratten schützte diese fast vollständig gegen Indomethacin-induzierte Magengeschwüre durch einen Mechanismus, der unabhängig von der Modulation der Säuresekretion, des Mucingehaltes oder der Pepsinaktivität war, jedoch über die Aufrechterhaltung von NO-Schleimhaut. Andererseits, die Vorbehandlung von Ratten mit den NOS-Inhibitoren L-NAME (50 mg/kg), einem nicht-selektiven konstitutiven Stickoxid-Synthase/induzierbaren Stickoxid-Synthase (cNOS / iNOS) -Inhibitor oder dem selektiven iNOS-Inhibitor Aminoguanidin (AMG) (50 mg/kg) verschlechtert den Ulkusindex (die Summe der Länge (mm) aller Läsionen in der Fundusregion, Abb. 3). Zur Unterstützung der anti-ulcerogenen Wirkung von L-Arginin haben Lazaratos et al. und Jimenez et al. die schützende Rolle von L-Arginin gegen die ulzerogene Wirkung von Endothelin-1 bzw. Ibuprofen aufgezeigt.
 Abb. 3. Ulkusindex (mm) von normalen, Indomethacin-, L-NAME-, Aminoguanidin- und L-Arginin-behandelten Ratten. Die Ergebnisse sind Mittelwerte ± SEM von 6-10 Tieren. ** Signifikante Unterschiede zu Indomethacin bei p <0,01.
Abb. 3. Ulkusindex (mm) von normalen, Indomethacin-, L-NAME-, Aminoguanidin- und L-Arginin-behandelten Ratten. Die Ergebnisse sind Mittelwerte ± SEM von 6-10 Tieren. ** Signifikante Unterschiede zu Indomethacin bei p <0,01.
Die Berichte haben sich nicht die Rolle von NO auf den Magenschutz beschränkt, sondern auch die Beschleunigung der Heilung von Geschwüren diskutiert. Konturek et al. haben gezeigt, dass Glyceryltrinitrat zur Heilung von Geschwüren fähig ist und, dass die Unterdrückung der NO-Synthese zu einer beeinträchtigten Heilung von Geschwüren führt. Es ist möglich, dass NO die Regeneration von Geschwüren direkt beschleunigt, indem es das Wachstum glatter Muskeln fördert, wie von Hogaboam et al.
In einer kürzlich durchgeführten Studie (im Druck) haben wir den Effekt der NO-Modulation auf die Heilung von Magengeschwüren unter Verwendung der NO-Vorstufe getestet; L-Arginin, ein kompetitiver Inhibitor von NOS, L-NAME und dem NO-Donor; Nitroglycerin (NTG). Den Ratten wurde eine einzelne orale Dosis von Indomethacin (30 mg/kg) injiziert und dann 4 Stunden nach der Indomethacin-Injektion 7 Tage lang einmal täglich mit L-Arginin, NTG oder L-NAME behandelt. Die Untersuchung der Gesamtläsion und die histologische Beurteilung wurden durchgeführt. Der Magengewebeanteil von NO, PGE2 und Mucin wurde nachgewiesen. Zusätzlich wurden oxidative Stressmarker einschließlich Glutathion (GSH) und Lipidperoxide gemessen. Es wurde herausgefunden, dass L-Arginin und NTG die Heilung von Indomethacin-induzierten Geschwüren, wie in makroskopischen und histologischen Untersuchungen ersichtlich, beschleunigen, um normale Niveaus von NO und GSH wiederherzustellen und den durch Indomethacin induzierten Anstieg von PGE2 und Lipidperoxiden signifikant zu dämpfen. Auf der anderen Seite wurde herausgefunden, dass L-NAME die Schleimhautschädigung verschlimmert.
Tabelle 3. Grobe Untersuchung der Wirkung der Behandlung mit L-Arginin, NTG oder L-NAME auf Magengeschwüre durch Indomethacin bei Ratten induziert.
| Gruppen | Anzahl toter Ratten | Ulkus No. | Ulkus index (mm) | Ulkus score |
|---|---|---|---|---|
| Control | 0 | 0 | – | – |
| Indomethacin | 3 | 13.25 ± 0.75 | 19.0 ± 1.45 | 3.62 ± 0.26 |
| Indomethacin + l-arginine | 1 | 0 | – | – |
| Indomethacin + NTG | 2 | 0 | – | – |
| Indomethacin + l-NAME | 5 | 17.11 ± 0.65 | 23.2 ± 1.15 | 4.55 ± 0.17 |
Das Magengeschwür wurde durch eine einmalige orale Injektion von Indomethacin (30 mg/kg) induziert, und dann 4 Stunden später, wurde die Medikamente täglich für 1 Woche wie folgt verabreicht: L-Arginin (200 mg/kg), NTG (1 mg/kg) und L-NAME (15 mg/kg). Die Messungen wurden 7 Tage später durchgeführt. Die angegebenen Werte sind Mittelwerte von 10-15 Beobachtungen ± SEM. Ulkusindex = Summe der Längen aller Läsionen in jedem Magen; Ulkus Score zeigt die Schwere der Magenläsion, wobei 1 (ulzerierten Bereich 1-6 mm2), 2 (ulzerierten Bereich 7-12 mm2), 3 (ulzerierten Bereich 13-18 mm2), 4 (ulzerierten Bereich 19-24 mm2) und 5 (ulzerierter Bereich> 24 mm2). Parallel dazu haben Brzozowski et al. gezeigt, dass die intragastrische Verabreichung von L-Arginin (32,5 bis 300 mg/kg/Tag) die Heilungsrate von Essigsäure-induzierten Geschwüren in einer dosisabhängigen Weise erhöhte, während D-Arginin nicht wirksam war.
In sehr wenigen Artikeln wurde die Wirkung einer L-Arginin-Supplementation auf die ZNS-Funktion untersucht. Die akkumulierenden Beweise deuten jedoch darauf hin, dass NO bei der Gedächtnisbildung eine Rolle spielt. In vitro wird nach einer spezifischen Rezeptorstimulation NO aus einer postsynaptischen Quelle freigesetzt, um auf einem oder mehreren Neuronen präsynaptisch zu wirken. Dies führt zu einer weiteren Erhöhung der Freisetzung von Glutamat und folglich zu einer stabilen Zunahme der synaptischen Transmission, ein Phänomen, das als Langzeitpotenzierung bekannt ist. Es wird angenommen, dass dies mit der Speicherfunktion verbunden ist.
Tierexperimente deuten auch darauf hin, dass NO am Gedächtnis beteiligt ist, da die Hemmung der NO-Synthese in vivo das Lernverhalten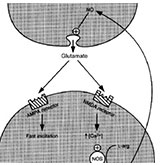
Abb. 5. Die Rolle von Stickstoffmonoxid bei der langfristigen Potenzierung der neuronalen Aktivität. Glutamat, das vom präsynaptischen Nervenende freigesetzt wird, aktiviert verschiedene Arten von Rezeptoren an den Dendriten des postsynaptischen Neurons. Unter normalen Bedingungen vermitteln die alpha-Amino-3-hydroxy-5-methyl-4-isoxazolpropionat (AMPA) -Rezeptoren die meisten Wirkungen von Glutamat. Während der hochfrequenten synaptischen Übertragung führt die Aktivierung von N-Methyl-d-aspartat (NMDA) -Rezeptoren jedoch zu einem Anstieg des intrazellulären Calciums, das die konstitutive Stickstoffmonoxid-Synthase (NOS) stimuliert. Das Stickstoffmonoxid (NO), das produziert wird, diffundiert zurück zum präsynaptischen Neuron, wo es die Freisetzung von Glutamat verstärkt. Die erhöhte Glutamatfreisetzung führt zu einer stärkeren Aktivierung von postsynaptischen Glutamatrezeptoren, wodurch die Wirksamkeit dieser Synapse erhöht wird. Pluszeichen weisen auf Stimulation hin, und L-Arg bedeutet L-Arginin.
L-Arginin (1,6 g/Tag) bei 16 älteren Patienten mit seniler Demenz hat sich als wirksam erwiesen, um die Lipidperoxidation zu reduzieren und die kognitive Funktion zu erhöhen. In ihrem jüngsten Bericht untersuchten Jing et al. die mögliche Rolle von L-Arginin bei der Alzheimer-Krankheit (AD) unter Berücksichtigung bekannter Funktionen für L-Arginin bei Atherosklerose, Redoxstress und dem Entzündungsprozess, Regulation der synaptischen Plastizität und Neurogenese sowie Modulation des Glucosestoffwechsels und der Insulinaktivität. Sie lieferten Hinweise darauf, dass L-Arginin eine wichtige Rolle beim Schutz vor altersbedingten degenerativen Erkrankungen, wie AD, spielen könnte. Weitere Untersuchungen sind erforderlich, um diesen unberührten Forschungsbereich abzudecken.
In einer offenen, randomisierten, limitierten Studie des Autors.
Bei 21 Probanden mit einem Alter zwischen 41 und 75 Jahren (14 zwischen 41 und 49 Jahren, 4 zwischen 50 und 59 Jahren, 2 zwischen 60 und 69 Jahren) wurden 28 Tage lang einmal in der Nacht 5 g/Tag L-Arginin-Base oral verabreicht , und 1 zwischen 70 und 79 Jahren), 16 waren Männer und 5 Frauen, 17 waren Nichtraucher und 4 Raucher, und 18 der 21 Patienten nahmen andere Medikationen, um entweder Bluthochdruck, Myokardischämie, Diabetes, gastroösophagealen Reflux zu kontrollieren, Krankheit (GERD) und Übersäuerung, Hypothyreose, Neuritis oder Rheumatoide. Alle rekrutierten Personen gaben eine schriftliche Einverständniserklärung, die den Grundsätzen der Helsinki-Erklärung entsprach.
Den Probanden wurde wöchentlich ein Fragebogen für 4 Wochen ausgehändigt. Den Probanden wurde empfohlen, ihren Gesundheitszustand vor und nach der Einnahme von L-Arginin zu schreiben. Der Fragebogen umfasste 30 Punkte bezüglich ihrer mentalen, muskulären, sexuellen, Kreislauf-, GIT- und anderen Funktionen während der vierwöchigen Verabreichung. Die Bewertung wurde von 1 bis 5 aufgezeichnet; 1 war eine bemerkenswerte Verbesserung, 2 war eine leichte Verbesserung, 3 kein Unterschied, 4 war schlechter als zuvor und 5 war nicht anwendbar. Die Probanden wurden auch aufgefordert, Nebenwirkungen, die während der Verabreichung der Ergänzung auftraten, zu melden. Darüber hinaus wurden sie gefragt, ob sie den Zuschlag nach Beendigung der Studie weiter einnehmen wollten. Die Tabellen 4 und 5 fassen die wichtigsten Informationen dieser Pilotstudie zusammen.
| Feature | % der Fälle (total = 21 Fälle) | ||
|---|---|---|---|
| Mental Fähigkeit | Bemerkenswerte Verbesserung | Leichte Verbesserung | Keine Veränderung |
| Konzentrationsfähigkeit | 55 | 35 | 10 |
| Speicherabruf | 55 | 35 | 10 |
| Verzögerung in der geistigen Erschöpfung | 75 | 15 | 10 |
| Verringerung der Schwere von Angst und Stress | 60 | 20 | 20 |
| Verringerung der Nervosität | 72 | 21 | 60 |
| Tiefschlaf | 80 | 10 | 10 |
| Allgemeine Stimmung | 70 | 25 | 5 |
| Muskuläre Leistung | 75 | 5 | 20 |
| Verzögerung der Muskelerschöpfung | 60 | 15 | 25 |
| Sexuelle Leistung bei Männern | 54 | 33 | 13 |
| Insgesamt Gefühl des Wohlbefindens | 65 | 20 | 15 |
Tabelle 4. Auffälligste Beobachtungen der Probanden am Ende der 4-Wochen-Studie.
1. Anpassung des Blutdrucks bei leichter Hypertonie.
2. Hohe Energie, besonders morgens beim Aufwachen.
3. Klare Meinung.
4. Ausdauer und Widerstand gegen Depressionen und Angstzustände.
5. Anstieg der Urinproduktion.
6. Verbesserung des Haar- und Nagelwachstums und der Härte.
7. Verbesserung der Hautbeschaffenheit und des Aussehens.
8. Zunahme der Nachtträume.
9. Verbesserung der Durchblutung und Temperatur der Extremitäten.
10. Verringerung der Übersäuerung.
11. Gesamtverbesserung des GIT-Systems und Defäkation.
12. Verbesserung der meisten lebenswichtigen Aktivitäten bei Diabetikern, einschließlich: Verringerung der Neuritis, Verbesserung des Glukosestoffwechsels, Verbesserung der Libido und der sexuellen Leistungsfähigkeit und Anpassung des Körpergewichts
Am Ende der Studie gab es in keinem der 21 Fälle Nebenwirkungen oder eine Verschlimmerung der Gesundheitsprobleme durch die Verabreichung von L-Arginin. Alle 21 Fälle wollten die Ergänzung nach Beendigung der Studie fortsetzen.
An der Wundheilung sind Thrombozyten, Entzündungszellen, Fibroblasten und Epithelzellen beteiligt. Alle diese Zelltypen sind in der Lage, NO zu produzieren, entweder konstitutiv oder als Reaktion auf inflammatorische Zytokine. NO, das sowohl von der iNOS als auch von der eNOS gebildet wird, spielt eine wichtige Rolle bei der Wundheilung von der Entzündungsphase bis zur Narbenbildung. NO hat zytostatische, chemotaktische und vasodilatatorische Wirkungen während der frühen Wundheilung, reguliert die Proliferation und Differenzierung verschiedener Zelltypen, moduliert die Kollagenablagerung und Angiogenese und beeinflusst die Wundkontraktion.
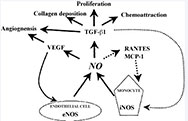 Abb. 4. Schematische Darstellung der hypothetischen Rollen von NO in der Wundheilung. Die Produktion von NO aus eNOS oder iNOS führt zur Modulation von Zytokinen (z. B. MCP-1, RANTES, VEGF und TGFb1), die wiederum die verschiedenen Facetten der Wundheilung modulieren (z. B. Chemoattraktion, Proliferation, Kollagenablagerung und Angiogenese).
Abb. 4. Schematische Darstellung der hypothetischen Rollen von NO in der Wundheilung. Die Produktion von NO aus eNOS oder iNOS führt zur Modulation von Zytokinen (z. B. MCP-1, RANTES, VEGF und TGFb1), die wiederum die verschiedenen Facetten der Wundheilung modulieren (z. B. Chemoattraktion, Proliferation, Kollagenablagerung und Angiogenese).
Erstmals wurde 1978 festgestellt, dass L-Arginin die Wundheilung verbessert. Seitdem konnte gezeigt werden, dass L-Arginin in der Nahrung sowohl bei Menschen als auch bei Tieren die Kollageneinlagerung und die Wundfestigkeit verbessert. Dieser Effekt kann zum Teil auf die nachfolgende Steigerung der Ornithinproduktion durch die Wirkung des Enzyms Arginase, einer Vorstufe von L-Prolin während der Kollagensynthese, zurückgeführt werden. Die direkte Rolle von NO als Cofaktor bei der Förderung der Wundheilung durch L-Arginin wurde ebenfalls beschrieben. L-Arginin könnte die Funktion von Immunzellen verbessern, indem es die Entzündungsreaktion an der Wundstelle reduziert.
Die heilende Wirkung von L-Arginin erstreckt sich auch auf Verbrennungen. Eine orale diätetische L-Argininsupplementierung von 100-400 mg/kg/Tag verkürzte die Reepithelisierungszeiten, erhöhte die Hydroxyprolinspiegel und beschleunigte die Synthese von reparativem Kollagen bei Ratten mit Verbrennungen. Verbrennungen erhöhen signifikant die Argininoxidation und die Schwankungen der Argininreserven. Totale parenterale Ernährung (TPN) erhöht die Umwandlung von Arginin in Ornithin und erhöht proportional die irreversible Argininoxidation. Dies macht Arginin bei Patienten mit schweren Verbrennungen, die eine totale parenterale Ernährung erhalten, bedingt wichtig.
Diabetes ist mit verminderten Arginin-Plasmaspiegeln und erhöhten Spiegeln des NOS-Inhibitors ADMA assoziiert. Es gibt Hinweise darauf, dass eine Argininsupplementierung ein wirksames Mittel zur Verbesserung der Endothelfunktion bei Patienten mit Diabetes mellitus (DM) sein könnte. Es wurde auch gezeigt, dass niedrig dosiertes intravenös verabreichtes Arginin die Insulinsensitivität bei adipösen Patienten, Typ-2-Diabetikern und gesunden Probanden verbessert. Arginin kann auch der Lipidperoxidation entgegenwirken und dadurch die mikroangiopathischen Langzeitkomplikationen von DM reduzieren.
In einer Doppelblindstudie konnte gezeigt werden, dass eine orale Argininsupplementierung (3 g dreimal täglich über einen Monat) die periphere und hepatische Insulinsensitivität bei Patienten mit Typ 2 Diabetes mellitus signifikant verbesserte, aber nicht vollständig normalisierte. Außerdem reguliert L-Arginin die Insulinfreisetzung über NO-abhängige und NO-unabhängige Wege.
L-Arginin wird ein ergogenes Potenzial nachgesagt. Athleten haben Arginin aus drei Hauptgründen eingenommen:
In einer Doppelblindstudie wurde die Wirkung einer vierwöchigen Behandlung mit Argininaspartat bei 21 Sportlern untersucht. Die behandelte Gruppe zeigte einen Anstieg der maximalen Sauerstoffaufnahme sowie eine signifikante Abnahme der Plasmalaktatkonzentration bei einer Arbeitsintensität von 200, 300 und 400 W (Lauftraining) auf dem Laufband im Vergleich zur Kontrollgruppe. In einer anderen Studie führte die 8-wöchige orale Verabreichung von L-Arginin (3 g) an 20 männliche Probanden, die ein Trainingsprogramm mit Gewichten absolvierten, zu einer signifikanten Zunahme der Muskelkraft und -masse im Vergleich zur unbehandelten Gruppe.
Duchenne-Muskeldystrophie (DMD) ist eine tödliche X-chromosomale Erkrankung, die mit einem Dystrophin-Mangel einhergeht, der zu chronischen Entzündungen, Sarkolemmschäden und schwerer Degeneration der Skelettmuskulatur führt. Vor kurzem wurde die Verwendung von L-Arginin, dem Substrat der neuronalen Stickstoffmonoxidsynthase (nNOS), als pharmakologische Behandlung vorgeschlagen, um das dystrophische Muster der DMD abzuschwächen. Hnia et al. konnten zeigen, dass L-Arginin in mdx-Mäusen (einem Tiermodell der Duchenne-Muskeldystrophie) Entzündungen reduziert und die Muskelregeneration fördert. Die hemmende Wirkung von L-Arginin auf die NF-kappaB/Metalloproteinase-Kaskade reduziert die beta-Dystroglycan-Spaltung und transloziert Utrophin und nNOS im gesamten Sarkolemm. Es gibt Hinweise darauf, dass L-Arginin Utrophin in Muskeln hochreguliert, was das Fehlen von Dystrophin bei DMD kompensieren könnte. Utrophin hat eine Homologie von über 80% mit Dystrophin.
Neben den oben genannten Vorteilen hat sich gezeigt, dass L-Arginin folgende Wirkungen besitzt:
Die nachgewiesenen Anti-Aging-Vorteile von L-Arginin sind vielversprechender als alle bisher entdeckten pharmazeutischen oder nutrazeutischen Wirkstoffe.